COMPORTAMIENTO DE LOS GASES

Los gases están constituidos por pequeñas partículas llamadas moléculas, poseen masa pero tienen un volumen despreciable.
Debido a que las partículas de gas permanecen separadas, entre ellas no existen fuerzas de atracción o repulsión significativas y puede considerarse que se comportan como masas muy pequeñas.
Las partículas de gas están en continuo movimiento en dirección aleatoria y con frecuencia chocan unas con otras.
La energía cinética de las partículas puede ser convertida en calor o en otra forma de energía. La energía cinética total de las moléculas permanece constante si el volumen y la temperatura del gas no cambian, de igual forma, la presión de un gas es constante si el volumen y la temperatura con cambian.
Debido a que las partículas de gas permanecen separadas, entre ellas no existen fuerzas de atracción o repulsión significativas y puede considerarse que se comportan como masas muy pequeñas.
Las partículas de gas están en continuo movimiento en dirección aleatoria y con frecuencia chocan unas con otras.
La energía cinética de las partículas puede ser convertida en calor o en otra forma de energía. La energía cinética total de las moléculas permanece constante si el volumen y la temperatura del gas no cambian, de igual forma, la presión de un gas es constante si el volumen y la temperatura con cambian.
PROPIEDADES DE LOS GASES
Debido a que resulta difícil medir la cantidad de un gas presente en un recipiente, esta cantidad se determina en forma indirecta, midiendo su presión, su volumen y su temperatura.
Presión atmosférica: es la presión que la atmósfera ejerce sobre la superficie de la tierra y sobre todos los seres que se encuentran en ella. A nivel del mar la presión atmosférica es
de 760 mmHg, que equivalen a 1 atmósfera de presión.
Debido a que resulta difícil medir la cantidad de un gas presente en un recipiente, esta cantidad se determina en forma indirecta, midiendo su presión, su volumen y su temperatura.
- Volumen: es el espacio en el cual se mueven las moléculas que forman un gas y está determinado por el volumen del recipiente que lo contiene, la unidad empleada para su medición es el litro (L) o el metro cubico (m3).
- Presión: se define como la aplicación de una fuerza, que se distribuye sobre un área determinada, en un gas las moléculas al moverse continuamente y a altas velocidades, no solo chocan entre si, sino que también lo hacen con las paredes del recipiente que las contiene. La presión se calcula mediante la expresión Presión= Fuerza/ Área P=F/A.
Presión atmosférica: es la presión que la atmósfera ejerce sobre la superficie de la tierra y sobre todos los seres que se encuentran en ella. A nivel del mar la presión atmosférica es
de 760 mmHg, que equivalen a 1 atmósfera de presión.
- Temperatura: es la expresión de la energía cinética de las moléculas que componen el gas y depende de su velocidad.
LEYES DE LOS GASES IDEALES
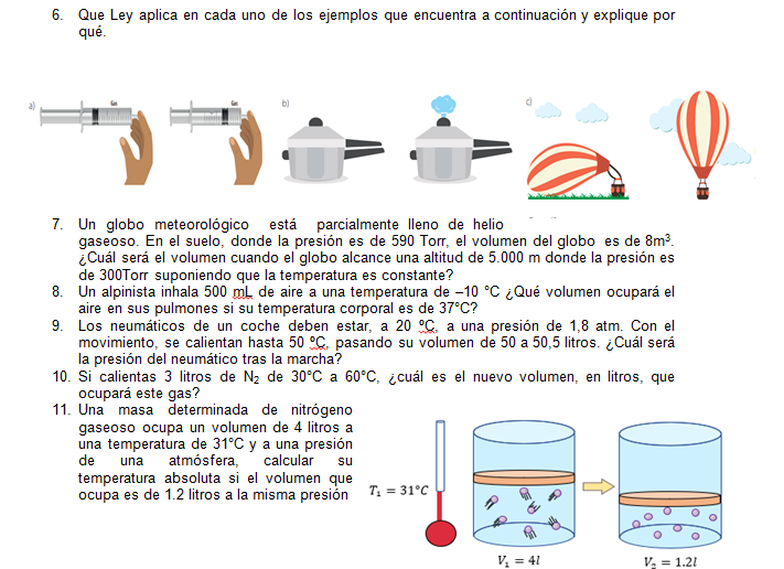
Los gases se comportan de forma diferente que los sólidos y líquidos, por ejemplo el volumen de un gas puede cambiar debido a la presión, pero el volumen de un sólido o un líquido generalmente no. Las leyes de los gases describen como afectan el comportamiento de los gases, las variables como la presión, volumen y temperatura.
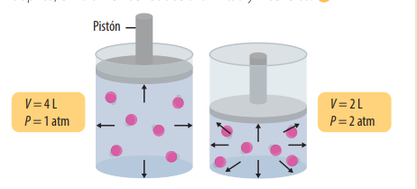
1. Ley de Boyle: dice que: Si la temperatura de cierta cantidad de gas se mantiene constante, el volumen (V) de éste cambia inversamente con la presión (P) del gas. Ya que la temperatura se mantiene constante durante este proceso, a éste se le denomina proceso isotérmico. Se puede observar que a medida que aumenta la presión ejercida sobre el gas, su volumen disminuye (se comprime). Es decir, entre estas dos variables se da una relación inversamente proporcional: mientras la una aumenta, la otra disminuye. Esto puede ser expresado así: P₁V₁ = P₂V₂.
Los gases se comportan de forma diferente que los sólidos y líquidos, por ejemplo el volumen de un gas puede cambiar debido a la presión, pero el volumen de un sólido o un líquido generalmente no. Las leyes de los gases describen como afectan el comportamiento de los gases, las variables como la presión, volumen y temperatura.
1. Ley de Boyle: dice que: Si la temperatura de cierta cantidad de gas se mantiene constante, el volumen (V) de éste cambia inversamente con la presión (P) del gas. Ya que la temperatura se mantiene constante durante este proceso, a éste se le denomina proceso isotérmico. Se puede observar que a medida que aumenta la presión ejercida sobre el gas, su volumen disminuye (se comprime). Es decir, entre estas dos variables se da una relación inversamente proporcional: mientras la una aumenta, la otra disminuye. Esto puede ser expresado así: P₁V₁ = P₂V₂.
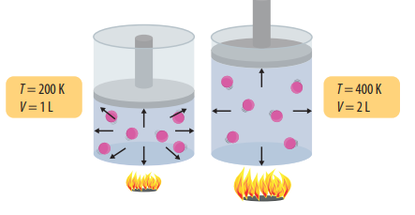
2. Ley de Charles: dice que: Si la presión de cierta cantidad de gas se mantiene constante, el volumen (V) de éste guarda una relación directamente proporcional con su temperatura (T). Ya que la presión se mantiene constante durante este proceso, a éste se le denomina proceso Isobárico. Esto puede ser expresado así: V₁/T₁ = V₂/T₂, debido a que si se mide la temperatura (T) y el volumen (V) al inicio (estado 1) y al final del proceso (estado 2), se puede encontrar que habrán aumentado en la misma proporción, así que la división entre esos dos valores será una constante. La temperatura se expresa en kelvin. K=0C + 273
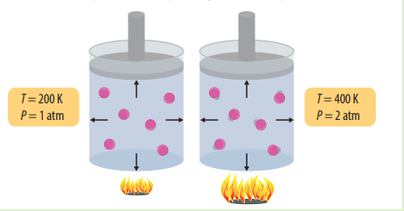
3. Ley de Gay-Lussac: dice que: Si el volumen de cierta cantidad de gas se mantiene constante, la presión (P) de éste guarda una relación directamente proporcional con la temperatura (T). Ya que el volumen se mantiene constante durante este proceso, a éste se le denomina proceso isocórico. Esto puede ser expresado así: P₁/T₁ = P₂/T₂, debido a que si medimos la Presión (P) y la Temperatura (T) al inicio (estado 1) y al final del proceso (estado 2), podremos encontrar que habrán aumentado en la misma proporción, así que la división entre esos dos valores será una constante.
4. Ley combinada o general de los gases: Es la suma de las leyes de Boyle, Charles y gay Lussac, esta ley plantea que: El volumen de un gas es directamente proporcional a la temperatura e inversamente proporcional a la presión se expresa asi: P1 V₁ / T1=P2 V2 / T₂