EL ÁTOMO Y SU EVOLUCIÓN.
Los filósofos griegos discutieron mucho sobre la naturaleza de la materia y concluyeron que el mundo era más sencillo de lo que parecía.
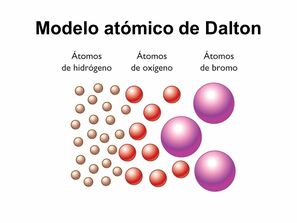
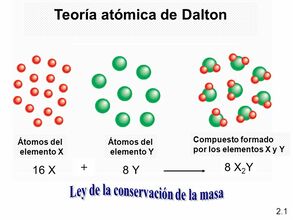
En el siglo V a.C., Leucipo pensaba que sólo había un tipo de materia. Sostenía, además, que si dividíamos la materia en partes cada vez más pequeñas, acabaríamos encontrando una porción que no se podría seguir dividiendo. Un discípulo suyo, Demócrito, bautizó a estas partes indivisibles de materia con el nombre de átomos, término que en griego significa “que no se puede dividir”.
Los filósofos griegos discutieron mucho sobre la naturaleza de la materia y concluyeron que el mundo era más sencillo de lo que parecía.
En el siglo V a.C., Leucipo pensaba que sólo había un tipo de materia. Sostenía, además, que si dividíamos la materia en partes cada vez más pequeñas, acabaríamos encontrando una porción que no se podría seguir dividiendo. Un discípulo suyo, Demócrito, bautizó a estas partes indivisibles de materia con el nombre de átomos, término que en griego significa “que no se puede dividir”.
Los filósofos griegos discutieron mucho sobre la naturaleza de la materia y concluyeron que el mundo era más sencillo de lo que parecía.
En el siglo V a.C., Leucipo pensaba que sólo había un tipo de materia. Sostenía, además, que si dividíamos la materia en partes cada vez más pequeñas, acabaríamos encontrando una porción que no se podría seguir dividiendo. Un discípulo suyo, Demócrito, bautizó a estas partes indivisibles de materia con el nombre de átomos, término que en griego significa “que no se puede dividir”.
Los filósofos griegos discutieron mucho sobre la naturaleza de la materia y concluyeron que el mundo era más sencillo de lo que parecía.
En el siglo V a.C., Leucipo pensaba que sólo había un tipo de materia. Sostenía, además, que si dividíamos la materia en partes cada vez más pequeñas, acabaríamos encontrando una porción que no se podría seguir dividiendo. Un discípulo suyo, Demócrito, bautizó a estas partes indivisibles de materia con el nombre de átomos, término que en griego significa “que no se puede dividir”.
MODELO ATÓMICO DE RUTERFORD

En 1911, el físico y químico Ernest Rutherford y sus colaboradores bombardearon una fina lámina de oro con partículas alfa (positivas), procedentes de un material radiactivo, a gran velocidad. El experimento permitió observar el siguiente comportamiento en las partículas lanzadas:
La mayor parte de ellas atravesaron la lámina sin cambiar de dirección, como era de esperar.
Algunas se desviaron considerablemente.
La mayor parte de ellas atravesaron la lámina sin cambiar de dirección, como era de esperar.
Algunas se desviaron considerablemente.
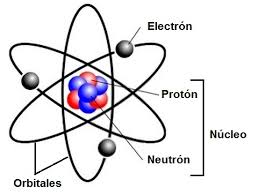
Unas pocas partículas rebotaron hacia la fuente de emisión.En el modelo de Rutherford: La carga positiva está concentrada en un núcleo central, de manera que las partículas positivas que pasan muy cerca de él se desvían bastante de su trayectoria inicial y sólo aquellas pocas que chocan directamente con el núcleo regresan en la dirección de la que proceden.
El Modelo de Rutherford establecía:
El átomo tiene un núcleo central en el que están concentradas la carga positiva y prácticamente toda la masa.
La carga positiva de los protones es compensada con la carga negativa de los electrones, que se hallan fuera del núcleo. El núcleo contiene, por tanto, protones en un número igual al de electrones del átomo.
Los electrones giran a gran velocidad alrededor del núcleo y están separados de éste por una gran distancia.
Rutherford supuso que el átomo estaba formado por un espacio fundamentalmente vacío, ocupado por electrones que giran alrededor de un núcleo central muy denso y pequeño.
Este modelo logró explicar el experimento de Rutherford con partículas alfa y otras observaciones, pero comenzó a ser inadecuado para interpretar nuevos conocimientos teóricos y experimentales.
Según los físicos una partícula cargada y en movimiento debería emitir energía de manera continua.
Si se aplica este concepto al modelo atómico de Rutherford, resultaría un átomo inestable: los electrones al girar irían perdiendo energía, cambiando la trayectoria circular por otra en forma de espiral, y finalmente serían atrapados por el núcleo.
El Modelo de Rutherford establecía:
El átomo tiene un núcleo central en el que están concentradas la carga positiva y prácticamente toda la masa.
La carga positiva de los protones es compensada con la carga negativa de los electrones, que se hallan fuera del núcleo. El núcleo contiene, por tanto, protones en un número igual al de electrones del átomo.
Los electrones giran a gran velocidad alrededor del núcleo y están separados de éste por una gran distancia.
Rutherford supuso que el átomo estaba formado por un espacio fundamentalmente vacío, ocupado por electrones que giran alrededor de un núcleo central muy denso y pequeño.
Este modelo logró explicar el experimento de Rutherford con partículas alfa y otras observaciones, pero comenzó a ser inadecuado para interpretar nuevos conocimientos teóricos y experimentales.
Según los físicos una partícula cargada y en movimiento debería emitir energía de manera continua.
Si se aplica este concepto al modelo atómico de Rutherford, resultaría un átomo inestable: los electrones al girar irían perdiendo energía, cambiando la trayectoria circular por otra en forma de espiral, y finalmente serían atrapados por el núcleo.
EXPERIMENTO DE RUTHERFORD
MODELO ATOMICO DE BOHR

Retomó en él la idea de la existencia del núcleo con carga positiva, zona central muy pequeña con respecto al volumen total del átomo donde se concentra la masa del mismo.
Para explicar por qué los electrones no caen al núcleo a medida que se mueven y van perdiendo energía, este científico utilizó el concepto de energía cuantizada, idea que fue desarrollada por Max Planck en 1900.
Según Planck, la energía puede ser liberada o absorbida solo en forma de “paquetes” a los que denominó cuantos (del latín quantum que significa cantidad).
El físico danés Niels Bohr realizó una serie de estudios de los que dedujo que los electrones de la corteza giran alrededor del núcleo describiendo sólo determinadas órbitas circulares. En el átomo, los electrones se organizan en capas y, en cada capa tendrán una cierta energía, llenando siempre las capas inferiores y después las superiores. La distribución de los electrones en las capas se denomina configuración electrónica y se realiza de la siguiente manera:
Para explicar por qué los electrones no caen al núcleo a medida que se mueven y van perdiendo energía, este científico utilizó el concepto de energía cuantizada, idea que fue desarrollada por Max Planck en 1900.
Según Planck, la energía puede ser liberada o absorbida solo en forma de “paquetes” a los que denominó cuantos (del latín quantum que significa cantidad).
El físico danés Niels Bohr realizó una serie de estudios de los que dedujo que los electrones de la corteza giran alrededor del núcleo describiendo sólo determinadas órbitas circulares. En el átomo, los electrones se organizan en capas y, en cada capa tendrán una cierta energía, llenando siempre las capas inferiores y después las superiores. La distribución de los electrones en las capas se denomina configuración electrónica y se realiza de la siguiente manera:
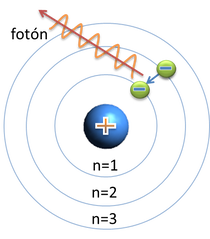
La 1ª capa puede contener, como máximo, 2 electrones.
La 2ª capa puede contener, como máximo, 8 electrones. Comienza a llenarse una vez que la 1ª ya está completa.
La 3ª capa puede contener, como máximo, 18 electrones. Comienza a llenarse una vez que la 2ª capa ya está completa.
La 2ª capa puede contener, como máximo, 8 electrones. Comienza a llenarse una vez que la 1ª ya está completa.
La 3ª capa puede contener, como máximo, 18 electrones. Comienza a llenarse una vez que la 2ª capa ya está completa.
MODELO ATOMICO ACTUAL

En 1926 Erwin Schrodinger propuso, una ligera modificación al modelo de Bohr, según la cual existían órbitas elípticas ademas de circulares permitiendo la existencia de niveles y subniveles de energía, describió el comportamiento del electrón en un átomo, considerando que la trayectoria de un electrón en el espacio es probabilística y los orbitales donde giran los electrones están determinados por cuatro parámetros llamados números cuánticos.
A diferencia del modelo de Böhr, la ecuación de Schrödinger se puede aplicar a átomos y moléculas distintos del hidrógeno, mostrando cómo está distribuida la nube electrónica alrededor del núcleo.
A diferencia del modelo de Böhr, la ecuación de Schrödinger se puede aplicar a átomos y moléculas distintos del hidrógeno, mostrando cómo está distribuida la nube electrónica alrededor del núcleo.
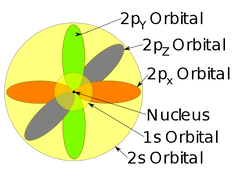
NÚMEROS CUÁNTICOS
El modelo mecánico-ondulatorio, describe cada electrón en términos de cuatro números cuánticos. Estos números permiten calcular la energía del electrón (cuantificar) y predecir el área alrededor del núcleo donde se puede encontrar el electrón. Los números cuánticos son:
El modelo mecánico-ondulatorio, describe cada electrón en términos de cuatro números cuánticos. Estos números permiten calcular la energía del electrón (cuantificar) y predecir el área alrededor del núcleo donde se puede encontrar el electrón. Los números cuánticos son:
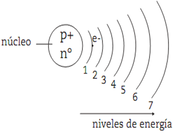
1. Número Cuántico Principal (n): Representa la capa o nivel de energía en la periferia del núcleo, donde se encuentra un electrón.
Mientras mayor sea n, mayor será la distancia que separa al electrón del núcleo y por lo tanto tendrá menor energía.

2. Número Cuántico Secundario (ℓ):
Corresponde al subnivel de energía. Toma valores que van desde 0 hasta n-1, que los identificamos como s, p, d, f
Corresponde al subnivel de energía. Toma valores que van desde 0 hasta n-1, que los identificamos como s, p, d, f
- Sharp (s) -> definida
- Principal (p) -> principal
- Difuse (d) -> difusa
- Fundamenta (f) -> fundamental
3. Número Cuántico magnético (mℓ) : Describe la orientación del orbital en el espacio. Para cada valor de l, ml puede tomar todos los valores enteros comprendidos entre -1 y +1. Asi, si l=2 los valores posibles de ml seran -2,-1,0,1,y 2.
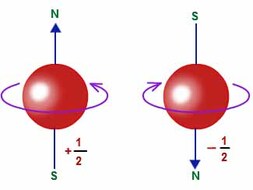
3. Número Cuántico de espin (ms): Un orbital puede albergar como máximo dos electrones. Dichos electrones se diferencian entre si por el sentido de giro sobre su eje. Cuando dos electrones ocupan el mismo orbital, sus sentidos de giro son opuestos. El numero cuantico ms puede tomar solamente dos valores +1/2 y -1/2 y se simbolizan con flechas. contrarias.