HISTORIA DE LA TABLA PERIODICA
En total se conocen más de 118 elementos que forman toda la materia que conoces. Algunos de esos 118 elementos se encuentran en la naturaleza formando parte de compuestos o bien como sustancias puras. Otros elementos fueron sintetizados artificialmente, sin embargo son muy inestables y, por lo tanto, existen durante muy pocos segundos. La organización y tabulación que hoy en día conocemos se le debe al químico ruso Henry Moseley. Este científico se basó en la recurrencia periódica y regular de las propiedades de los elementos en ese momento conocido. Esta organización del sistema periódico hizo posible la predicción de las propiedades de varios elementos que aún no habían sido descubiertos.

Actualmente la Tabla Periódica está ordenada en 7 filas horizontales llamadas periodos y 18 columnas verticales , llamadas grupos o familias.
GRUPOS O FAMILIAS QUÍMICAS: Los elementos están organizados en 18 columnas verticales llamadas grupos o familias químicas, los elementos de una familia química son similares en propiedades físicas y químicas, por lo cual reciben nombres particulares así:
GRUPO 1. (lA): metales alcalinos (excepto el hidrógeno).
GRUPO 2. (llA): metales alcalinoterreos.
GRUPO 13. (lllA): Familia del boro
GRUPO 14. (lVA): Familia del carbono
GRUPO 15. (VA): Familia del Nitrogeno.
GRUPO 16. (VlA): Familia del oxígeno.
GRUPO 17. (VllA): Familia de los halógenos.
GRUPO 18. (VlllA): gases nobles o inertes
ACTIVIDAD 1: Realiza el dibujo de la tabla periódica y pinta de diferentes colores los grupos representativos con su respectivo nombre.
GRUPOS O FAMILIAS QUÍMICAS: Los elementos están organizados en 18 columnas verticales llamadas grupos o familias químicas, los elementos de una familia química son similares en propiedades físicas y químicas, por lo cual reciben nombres particulares así:
GRUPO 1. (lA): metales alcalinos (excepto el hidrógeno).
GRUPO 2. (llA): metales alcalinoterreos.
GRUPO 13. (lllA): Familia del boro
GRUPO 14. (lVA): Familia del carbono
GRUPO 15. (VA): Familia del Nitrogeno.
GRUPO 16. (VlA): Familia del oxígeno.
GRUPO 17. (VllA): Familia de los halógenos.
GRUPO 18. (VlllA): gases nobles o inertes
ACTIVIDAD 1: Realiza el dibujo de la tabla periódica y pinta de diferentes colores los grupos representativos con su respectivo nombre.
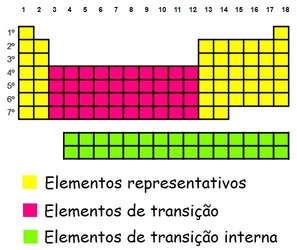
Diez grupos que ocupan las familias 3 al 12 son conocidos como elementos de transición. También se encuentran elementos adicionales normalmente colocados en la parte inferior de la tabla periódica, se llaman elementos de transición, divididos en dos series: lantánidos y actinidos.
ACTIVIDAD 2: Realiza el dibujo de la tabla periódica y pinta de rojo los elementos representativos, de verde los elementos de transición, sapote los lantánidos y amarillo los actinidos.
ACTIVIDAD 2: Realiza el dibujo de la tabla periódica y pinta de rojo los elementos representativos, de verde los elementos de transición, sapote los lantánidos y amarillo los actinidos.
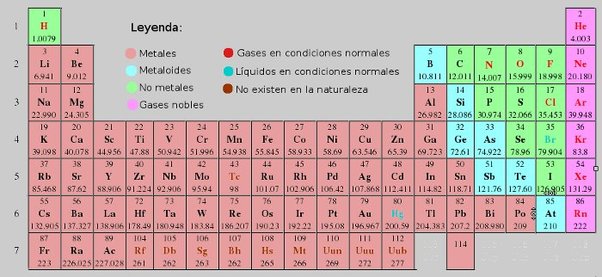
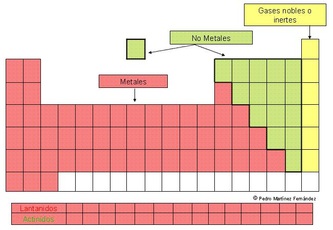
CARÁCTER METÁLICO DE LOS ELEMENTOS DE LA TABLA PERIÓDICA
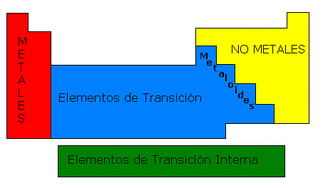
Los elementos están clasificados de acuerdo a su comportamiento metálico en:
METALES:
- Son buenos conductores del calor y la corriente eléctrica.
- Tienen una superficie lisa y brillante.
- Son sólidos a temperatura ambiente (excepto el mercurio y el galio).
- Pueden ceder electrones cuando se unen a otros elementos para formar un compuesto.
- Son maleables ( pueden extenderse y formar láminas delgadas) y dúctiles (pueden estirarse y formar hilos muy finos).
-Son elásticos y presentan resistencia a la ruptura.
- Se ubican en la parte izquierda de la tabla periódica.
- Algunos ejemplos de metales son el litio, el magnesio, el aluminio, el estaño, el oro y el mercurio.
NO METALES:
- Se pueden encontrar unidos a los metales o a otros no metales. También se pueden encontrar libres en su estado natural, como el azufre.
- Son malos conductores del calor y de la corriente eléctrica, por ello se emplean como aislantes.
- Presentan variedad de colores. No presentan brillo metálico.
- A temperatura ambiente pueden ser sólidos (carbono), líquidos (bromo) o gaseosos (oxígeno).
- Tienden a atraer los electrones cuando se unen a otros elementos para formar un compuesto.
- Por la dureza, no son maleables ni dúctiles.
- Se fragmentan con facilidad.
- Se ubican en la parte derecha de la tabla periódica.
-Algunos ejemplos de elementos no metales son el carbono, el oxigeno, neón o el azufre.
METALOIDES:
- tienen propiedades intermedias entre las de los metales y las de los no metales.
-Son semiconductores, por ende son muy usados en la electrónica.
-Son sólidos a temperatura ambiente.
-la mayoría presentan brillo metálico.
-La reactividad es muy variada.
-Son: el boro, silicio germanio, arsénico, antimonio, telurio, polonio y astato.
Los elementos están clasificados de acuerdo a su comportamiento metálico en:
METALES:
- Son buenos conductores del calor y la corriente eléctrica.
- Tienen una superficie lisa y brillante.
- Son sólidos a temperatura ambiente (excepto el mercurio y el galio).
- Pueden ceder electrones cuando se unen a otros elementos para formar un compuesto.
- Son maleables ( pueden extenderse y formar láminas delgadas) y dúctiles (pueden estirarse y formar hilos muy finos).
-Son elásticos y presentan resistencia a la ruptura.
- Se ubican en la parte izquierda de la tabla periódica.
- Algunos ejemplos de metales son el litio, el magnesio, el aluminio, el estaño, el oro y el mercurio.
NO METALES:
- Se pueden encontrar unidos a los metales o a otros no metales. También se pueden encontrar libres en su estado natural, como el azufre.
- Son malos conductores del calor y de la corriente eléctrica, por ello se emplean como aislantes.
- Presentan variedad de colores. No presentan brillo metálico.
- A temperatura ambiente pueden ser sólidos (carbono), líquidos (bromo) o gaseosos (oxígeno).
- Tienden a atraer los electrones cuando se unen a otros elementos para formar un compuesto.
- Por la dureza, no son maleables ni dúctiles.
- Se fragmentan con facilidad.
- Se ubican en la parte derecha de la tabla periódica.
-Algunos ejemplos de elementos no metales son el carbono, el oxigeno, neón o el azufre.
METALOIDES:
- tienen propiedades intermedias entre las de los metales y las de los no metales.
-Son semiconductores, por ende son muy usados en la electrónica.
-Son sólidos a temperatura ambiente.
-la mayoría presentan brillo metálico.
-La reactividad es muy variada.
-Son: el boro, silicio germanio, arsénico, antimonio, telurio, polonio y astato.
ACTIVIDAD 3:
- Consultar cuales son los elementos mas abundantes de la tierra y los elementos mas abundantes del universo.
- ¿Por qué los lantánidos son llamados como "tierras raras"? http://www.batanga.com/curiosidades/4694/que-son-las-tierras-raras
- Realiza un cuadro comparativo indicando las diferencias que hay entre:
a. elemento químico y compuesto químico.
b. Periodos y grupos
c. metáles y no metáles
- Escoge 5 elementos de la siguiente tabla periódica
http://herramientas.educa.madrid.org/tabla/ para completar la siguiente información:
Nombre: símbolo: punto de fusión: Número atómico: Punto de ebullición:
Peso atómico: grupo: periodo: densidad: usos:
- Consultar cuales son los elementos mas abundantes de la tierra y los elementos mas abundantes del universo.
- ¿Por qué los lantánidos son llamados como "tierras raras"? http://www.batanga.com/curiosidades/4694/que-son-las-tierras-raras
- Realiza un cuadro comparativo indicando las diferencias que hay entre:
a. elemento químico y compuesto químico.
b. Periodos y grupos
c. metáles y no metáles
- Escoge 5 elementos de la siguiente tabla periódica
http://herramientas.educa.madrid.org/tabla/ para completar la siguiente información:
Nombre: símbolo: punto de fusión: Número atómico: Punto de ebullición:
Peso atómico: grupo: periodo: densidad: usos:
PROPIEDADES DE LA TABLA PERIODICA
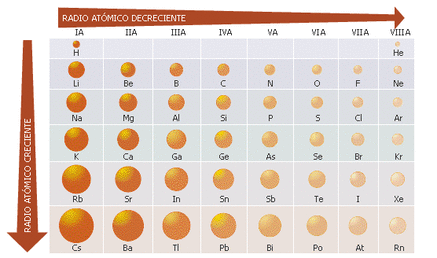
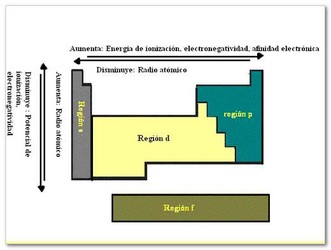
RADIO ATÓMICO
- Es relativo
- Depende de:
Nº de niveles energéticos: a mayor "n" mayor volumen, por lo tanto aumenta
al bajar en un grupo.
Número atómico "Z": cuanto mayor sea Z, en un mismo periodo, habrá mayor
atracción entre protones y eletrones y el átomo se contrae.
Disminuye de izda. a dcha. en un periodo.
- Es relativo
- Depende de:
Nº de niveles energéticos: a mayor "n" mayor volumen, por lo tanto aumenta
al bajar en un grupo.
Número atómico "Z": cuanto mayor sea Z, en un mismo periodo, habrá mayor
atracción entre protones y eletrones y el átomo se contrae.
Disminuye de izda. a dcha. en un periodo.

Energía de ionización:Energía requerida para mover un electrón de un átomo neutro. Aumenta con el grupo y diminuye con el período

Afinidad electrónica: Energía liberada cuando un átomo neutro captura un electrón para formar un ion negativo. Aumenta de izquierda a derecha y de abajo hacia arriba
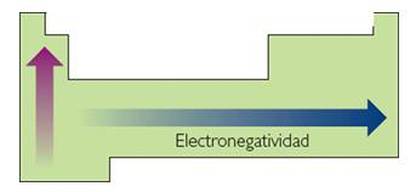
Electronegatividad de un elemento mide su tendencia a atraer hacia sí electrones, cuando está químicamente combinado con otro átomo. Cuanto mayor sea, mayor será su capacidad para atraerlos.
ACTIVIDADES PROPIEDADES DE LA TABLA PERIÓDICA:
1. Realiza en tu cuaderno las actividades que se encuentran en el siguiente link http://concurso.cnice.mec.es/cnice2005/93_iniciacion_interactiva_materia/curso/materiales/tabla_period/tabla.htm
2. Realiza en tu cuaderno las actividades que se encuentran en el siguiente link http://concurso.cnice.mec.es/cnice2005/93_iniciacion_interactiva_materia/curso/materiales/tabla_period/tabla2.htm
a. establece diferencias entre metales y no metales.
3. Realiza en tu cuaderno las actividades que se encuentran en el siguiente link http://concurso.cnice.mec.es/cnice2005/93_iniciacion_interactiva_materia/curso/materiales/tabla_period/tabla3.htm
1. Realiza en tu cuaderno las actividades que se encuentran en el siguiente link http://concurso.cnice.mec.es/cnice2005/93_iniciacion_interactiva_materia/curso/materiales/tabla_period/tabla.htm
2. Realiza en tu cuaderno las actividades que se encuentran en el siguiente link http://concurso.cnice.mec.es/cnice2005/93_iniciacion_interactiva_materia/curso/materiales/tabla_period/tabla2.htm
a. establece diferencias entre metales y no metales.
3. Realiza en tu cuaderno las actividades que se encuentran en el siguiente link http://concurso.cnice.mec.es/cnice2005/93_iniciacion_interactiva_materia/curso/materiales/tabla_period/tabla3.htm